Controle por bactérias de nematoides que atacam a cultura do tomate
Nematoides são responsáveis por graves prejuízos ao tomateiro e em situações de alta infestação podem levar à inviabilização do cultivo e da produção. Por isso a busca por
Na safra 2014/2015, em cultivos da safra e da safrinha, integrantes do Laboratório de Manejo Integrado de Pragas (LabMIP) da Universidade Federal de Santa Maria encontraram a Mosca-da-haste Melanagromyza sp. atacando soja nos municípios de Iporã do Oeste e Riqueza, em Santa Catarina e nos municípios de Boa Vista do Buricá, Cruz Alta e Três de Maio, no Rio Grande do Sul. Essas ocorrências surpreenderam pelo elevado grau de infestação e pela ampla distribuição na região. Com as ocorrências confirmadas em campo, o material foi coletado e a espécie de Melanagromyza (Diptera - Agromyzidae) presente na soja foi identificada. Essa identificação foi feita por técnicas morfológicas e moleculares, com a colaboração de entomologistas australianos. O Ministério da Agricultura, Pecuária e Abastecimento (MAPA) foi notificado da ocorrência da espécie em 01/07/2015. Antes disso, nos anos 1980 GASSEN et al. (1985), já tinham encontrado uma espécie do gênero Melanagromyza em Passo Fundo, Rio Grande do Sul e LINK et al. (2009) também reportaram a ocorrência da mosca-da-haste em lavouras de soja no município de São Francisco de Assis, também no estado gaúcho.
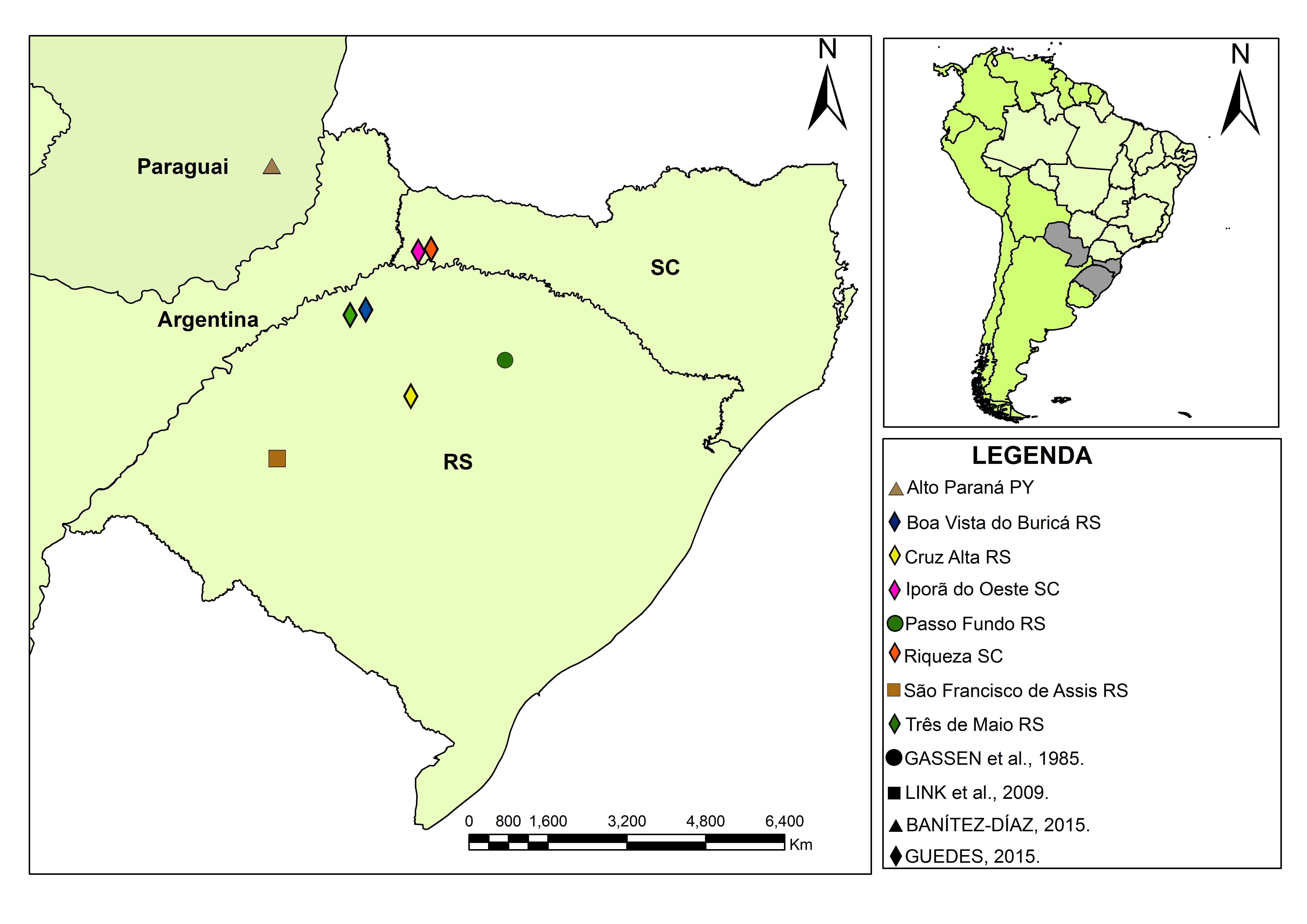
Também no Paraguai Melanagromyza sp. foi encontrada na última safra e notificada por BENÍTEZ-DÍAZ (2015). No Sul do Brasil, a ocorrência de larvas, pupas e adultos foi verificada desde os cultivos tardios da safra 2014/15, com maior incidência na safrinha do mesmo ano. Após a colheita da soja nos meses de maio, junho, julho, agosto e setembro de 2015 foram encontradas larvas, pupas e adultos da mosca-da-haste em soja espontânea no Rio Grande do Sul e em Santa Catarina.
Descrição: os adultos da mosca-da-haste são insetos pequeninos, medindo entre 2mm a 3 mm, de coloração negra e abdome verde metálico. Os ovos não são vistos. As larvas são de coloração amarelo-claro, translúcidas. Completamente desenvolvidas, medem até 4mm. As pupas são cilíndricas de coloração amarelada, passando a marrom e medem 2mm de comprimento.

Bioecologia
As fêmeas adultas ovipositam uma média de 170 ovos na face inferior das folhas em desenvolvimento, próximo às nervuras e na base do folíolo da soja e, inclusive, na folha unifoliolada. Prefere ovipositar em folhas tenras mas ocorrem posturas em trifólios recém abertos de plantas mais velhas (mesmo florescidas). As larvas eclodem entre 2 e 3 dias após a oviposição e iniciam a alimentação consumindo inicialmente o limbo foliar. Migram para uma nervura da folha e seguem broqueando rumo ao pecíolo e depois em direção a haste principal da planta. Passam por três ínstares larvais em um período de 8 a 11 dias. A fase de pupa dura entre 6 e 12 dias. Os adultos emergem dentro das galerias e abandonam a planta pelo orifício de emergência feito pela larva, antes de pupar. O ciclo de ovo-adulto, pode variar entre 16 a 26 dias, permitindo fazer mais de uma geração por cultivo. Na mesma planta são encontrados insetos em todas as fases do ciclo, ao mesmo tempo. Em plantas recém-emergidas as larvas fazem galerias descendentes, próximo ao segundo e ao primeiro nós, eventualmente broqueando através do colo, até a raiz principal. Ocorrem galerias ascendentes e descendentes dependendo da estatura e do período de infestação. Mesmo em plantas pouco desenvolvidas, espontâneas ou tigueras, podem ser encontradas várias larvas com infestação na etapa mais tardia da fase vegetativa e até na fase reprodutiva, tanto na haste principal como em ramificações próximo a esta.
Injúrias
Na fase adulta, a mosca se alimenta de fluídos celulares dos tecidos da epiderme não representando prejuízos à cultura. As larvas broqueiam o pecíolo e hastes fazendo galerias nos tecidos condutores, principalmente no xilema, podendo prejudicar o fluxo de água e nutrientes. Uma larva pode produzir uma galeria de 5,9cm até 13,4 cm de extensão. As plantas atacadas podem apresentar diminuição na estatura, número de flores, número de vagens, número de grãos, massa seca acumulada e redução da nodulação por Rhizobium.
Danos
As perdas dependem da região ou local de ocorrência da praga, do grau de infestação, da época de ataque da praga em relação ao estágio fenológico da cultura, da situação nutricional das plantas, da cultivar de soja, da época de semeadura, do uso de medidas de controle, entre outros fatores. Nas plantas perdas decorrem da redução do número e tamanho de nódulos fixadores de nitrogênio, da menor estatura de plantas, da área foliar, da redução da massa seca, do número de grãos e do rendimento da soja. As cinco primeiras semanas após a emergência das plântulas é o período de maior vulnerabilidade da soja à Melanagromyza sp.. A combinação desses fatores pode produzir perdas de 2% até 36% da produtividade da soja. Entretanto, qualquer estimativa de perdas para o Brasil seria precipitada, por não se conhecer a ocorrência da espécie nas extensas áreas de soja do Brasil e dos países vizinhos.
Detecção
A confirmação da ocorrência de Melanagromyza sp. não é possível pela visualização de sintomas externos da planta, exceto pela presença de orifícios de saída dos adultos. Tampouco é possível verificar a ocorrência de ovos com facilidade. A forma mais fácil de detectar a praga é pela visualização de larvas e/ou pupas ou pela presença de galerias na haste principal e ramificações da soja. A amostragem em lavouras deve ser feita arrancando plantas de soja ao acaso. Em seguida, seccionando as plantas com um corte transversal da haste na região do colo e separando a parte aérea das raízes. Com o auxílio de um canivete a planta deve ter a haste principal e ramificações laterais abertas longitudinalmente, de baixo para cima, expondo a medula e tecidos internos da haste, tornando possível verificar a ocorrência de larvas, pupas ou pupários vazios. Nesse momento é possível fazer a contagem das plantas atacadas, dos danos na haste principal e laterais e dos orifícios de saída. Em soja espontânea, a amostragem deve ser feita pela coleta de plantas isoladas dentro ou no entorno das lavouras, em estradas ou próximo a armazéns. O exame dessas plantas deve seguir os mesmos procedimentos recomendados para plantas cultivadas.

Monitoramento
O monitoramento é fundamental para detecção, quantificação e localização da ocorrência de Melagromyza sp na cultura da soja. Logo após a emergência da soja é possível constatar as ocorrências precoces da praga. Essas ocorrências são facilmente comprovadas pelo exame das plantas, presença de galerias e de larvas e/ou pupas. Mais tarde é possível pela presença de orifícios de saída localizados abaixo da região de inserção dos cotilédones. Em ataques mais tardios pela presença de orifícios de saída do adulto, acima da região cotiledonar.
Métodos de controle
Nas regiões do mundo onde a praga tem maior importância econômica para a cultura da soja, as medidas de controle mais importantes são o controle cultural, com cultivares resistentes e da semeadura fora dos picos populacionais da praga. O controle biológico também é mencionado como uma das estratégias para reduzir o impacto da praga. Há muitas referências da avaliação e do uso de inseticidas aplicados às sementes ou em pulverizações foliares. Nas condições do Brasil, seguramente o tratamento de sementes vai ser a estratégia mais adotada para o controle da praga, por já ser amplamente utilizado e pela ocorrência da praga na fase inicial da soja. Já a combinação do tratamento de sementes com pulverizações foliar é referido como a forma mais efetiva de controle da praga.
Perspectivas de manejo da praga
No Brasil, ainda não se conhece a ação de Melanagromyza sp. sobre as cultivares nacionais, com também o impacto do controle biológico natural e o efeito controle químico praticado para outras pragas da soja brasileira. É urgente e fundamental a avaliação da reação das cultivares à Melanagromyza sp., para ser somada a outras estratégias e integradas a outras medidas de controle desta praga. Essas e outras demandas técnico-científicas já estão sendo pesquisadas pelo LabMIP - UFSM, em colaboração com colegas da Austrália e do Paraguai.
O artigo foi matéria de capa da edição 197 da Cultivar Grandes Culturas, em outubro de 2015.

Receba por e-mail as últimas notícias sobre agricultura