Sim, é possível germinar seu cultivo com irrigação por gotejamento subterrâneo
Por Willian Damas, Especialista Agronômico Netafim
A mosca-branca (Bemisia tabaci) é uma praga polífaga que se alimenta de mais de 600 plantas, entre plantas cultivadas e não cultivadas. No Brasil, por muito tempo, foi considerada uma praga ocasional na cultura da soja, mas em 2019 foi eleita pelo Ministério da Agricultura, Pecuária e Abastecimento (MAPA) uma praga-chave nas culturas da soja, algodão e feijão. O inseto apresenta diferentes biótipos, ou raças, sendo que o Biótipo B, e o de maior ocorrência no Brasil.
O inseto causa danos diretos e indiretos às plantas, tanto na fase jovem (ninfas) quanto na fase adulta. Os danos diretos são causados pela sucção de seiva e injeção de toxinas, que ocasionam distúrbios fisiológicos nas plantas, como murcha e queda prematura das folhas. Os danos indiretos, são causados pela transmissão de doenças causados por vírus, uma vez que esse inseto pode transmitir mais de 130 espécies de vírus. Entre elas, a transmissão da doença conhecida como “necrose da haste da soja”, causada pelo vírus Cowpea mild mottle virus (CpMMV), que causam escurecimento do pecíolo, necrose da haste, queima do broto e deformidade nos grãos, reduzindo drasticamente sua produtividade.
Ademais, durante a alimentação, os insetos excretam grande quantidade de substâncias açucaradas, que servem de alimento para o crescimento do fungo Capnodium sp., causador da fumagina. Ao crescer sobre a secreção açucarada, o fungo forma uma cobertura escura sobre as folhas, o que reduz a capacidade fotossintética das plantas e, consequentemente, a redução da produtividade das culturas. As perdas de produção provocadas pela mosca-branca variam de acordo com a cultura e densidade populacional, podendo chegar a 100% em casos extremos, principalmente se há transmissão de viroses. Segundo a Aprosoja 2018, as perdas de soja no Mato Grosso na safra 2016/17 foram estimadas em 5 a 6 sacas/ha.
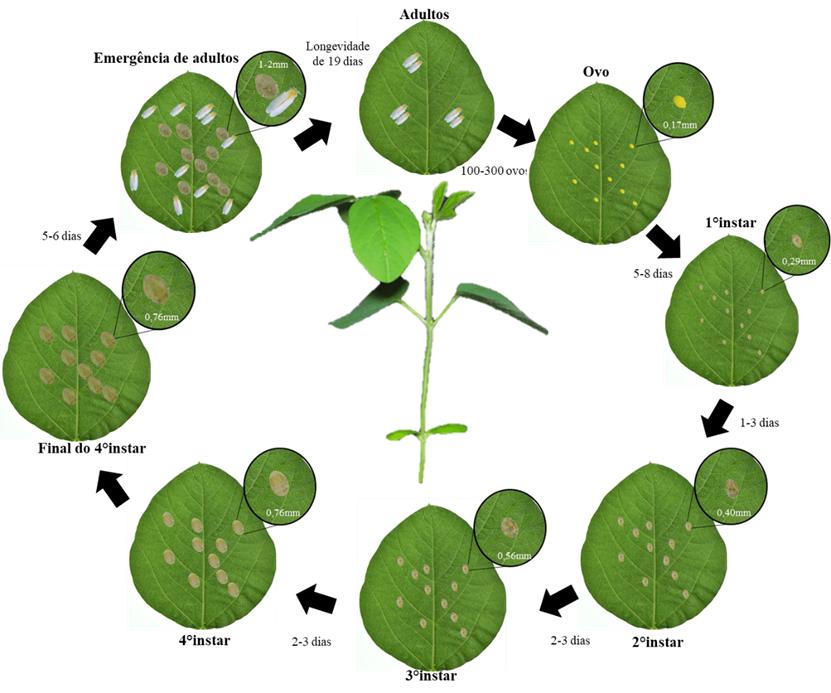
A mosca-branca é um inseto pertencente à ordem Hemiptera (Família:Aleyrodidae), cujo ciclo biológico se divide nas fases de ovo, ninfa e adulto. Esse inseto pode ter de 11 a 15 gerações/ano, dependendo das condições ambientais. Geralmente, macho e fêmea ficam pareados no momento da cópula (Figura 1). Cada fêmea pode colocar de 100 a 300 ovos durante sua longevidade, que pode ser de até 19 dias.
Os ovos apresentam formato alongado de cor amarela a alaranjada e medem 0,17 mm. Passados 5 a 8 dias da postura, as ninfas de primeiro estádio (ínstar) eclodem e deslocam na folha até achar um sítio de alimentação (Figura 1). Decorridos mais 1 a 3 dias, as ninfas mudam para o segundo ínstar, estádio no qual os pares de pernas são atrofiados. Após 2 a 3 dias, as ninfas mudam para o terceiro ínstar, que logo é sucedido pelo quarto ínstar, quando as ninfas apresentam dois pontos avermelhados correspondentes aos olhos dos adultos em formação. A emergência dos adultos ocorre entre 5 a 6 dias. Portanto, o ciclo de ovo a adulto pode levar de 15 a 26 dias, dependendo da temperatura, da umidade relativa do ar e de propriedades relativas ao hospedeiro.
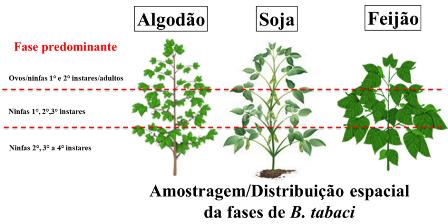
A tomada de decisão para o controle de mosca branca deve ser baseada em amostragens e levantamentos do número de insetos na área. A mosca branca apresenta uma distribuição uniforme na lavoura, assim, a sua amostragem pode ser realizada de forma aleatória, seguindo padrão de caminhamento que englobe toda a área de cultivo. O tipo de caminhamento mais utilizado é o em zigue-zague e os números de pontos amostrais podem variar de acordo com o tamanho da área. É recomendado que quantifique todas as fases do desenvolvimento do inseto (ovos, ninfas e adultos), no terço superior das plantas, local onde concentram-se todas as fases de desenvolvimento do inseto (Figura 2).
O nível de controle (NC) da mosca branca varia de acordo com a cultura, sendo diferente para algodão, soja e feijão. Na cultura do algodão, é recomendável entrar com o controle quando a praga atingir 60 % das plantas com adultos ou 40 % das plantas com ninfas. No caso da soja, é recomendável entrar com controle quando a densidade populacional atingir entre 5 a 10 ninfas ou adultos por folíolo. Já no caso de feijão, o nível de controle baseia-se na presença de 1 inseto/planta, uma população baixa devido ao inseto ser vetor do mosaico dourado do feijoeiro.
O controle microbiano para mosca-branca tem sido realizado com a utilização dos fungos entomopatogênicos Beauveria bassiana e Cordyceps (anteriormente=Isaria) fumosorosea. Atualmente, existem 37 produtos microbianos para controle de mosca branca registrados no MAPA, sendo 34 produtos à base de Beauveria bassiana e 3 produtos à base de Cordyceps fumosorosea. No campo, esses fungos têm sido aplicados tanto em combinação com produtos químicos quanto em aplicações isoladas.
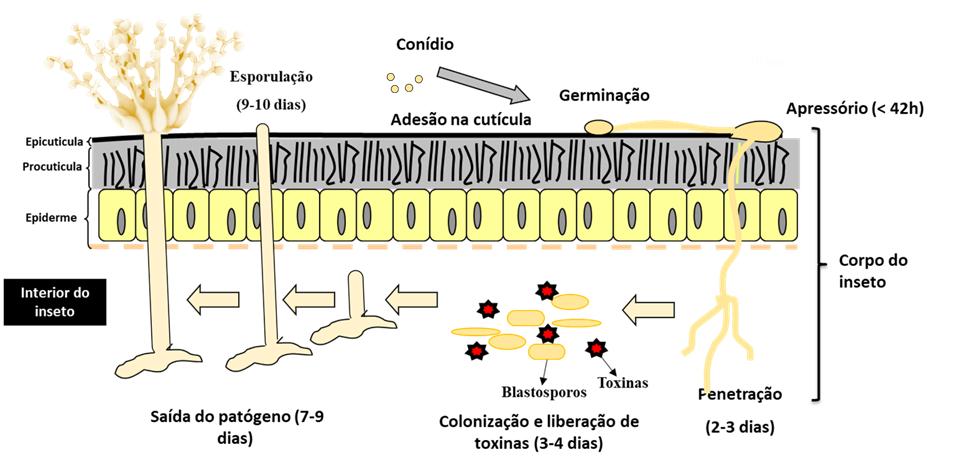
A ação de fungos entomopatogênicos (modo de ação) no controle da praga, inicia-se com a adesão dos conídios ao tegumento e posterior penetração no corpo do inseto (Figura 3). Os conídios aderidos no corpo do inseto germinam em poucas horas. Para a germinação, os conídios necessitam de condições ambientais favoráveis (“alta umidade”, >65%; temperatura de 25-30 °C e “baixa radiação solar”). A germinação do conídio resulta na formação de uma estrutura chamada “tubo germinativo”, que desenvolve e forma o “apressório”, estrutura de fixação e penetração do fungo. O apressório também libera enzimas “quitinases e lipases” que degradam a cutícula do inseto, favorecendo a penetração para o interior do corpo da praga. Dentro do inseto, o fungo passa a produzir toxinas que são liberadas na hemolinfa do inseto (corrente sanguínea do inseto). À medida que o fungo desenvolve, ele consome todos os nutrientes do corpo do inseto, processo que culmina no rompimento do tecido do inseto no sentido oposto (saída do patógeno), produzindo novos conídios (Figura 4). Esse processo é chamado “esporulação” e só ocorre em condições ambientais de alta umidade e temperatura entre 22 e 30 °C. Com a esporulação, os conídios são disseminados pelo vento, água ou mesmo por insetos e podem provocar a morte de outros insetos sadios não atingidos na aplicação, aumentando ainda mais a eficácia de controle.
O ponto chave para obter alta eficiência no controle de mosca branca com a aplicação de fungos entomopatogênicos é ter cuidados com tecnologia de aplicação do produto (principalmente com a cobertura da pulverização, pois “o fungo funciona por contato”) e a compatibilidade com os produtos químicos em mistura. Para determinar a área de cobertura podemos utilizar de tecnologias já disponíveis, como a tecnologia Check life (Kimberlit/ Bionat) ou mesmo papel hidrossensível. A tecnologia Check life fundamenta-se na utilização de adjuvante específico colocado na calda de pulverização. Os locais atingidos pela calda contendo adjuvante mais os microrganismos ficam de coloração fluorescentes (Figura 5, direita). No entanto, essa verificação de cobertura/deposição só é possível com observação da folha em equipamento específico (Check life). Folhas sem o equipamento, não é possível verificar a área de cobertura (Foto 5 da esquerda). Quanto melhor for a área de cobertura, melhor é a eficiência de controle. A compatibilidade de produtos químicos com os fungos entomopatogênicos é de fundamental importância para evitar a morte dos conídios no tanque de pulverização. Portanto, deve-se evitar a mistura com fungicidas químicos e produtos danosos aos conídios na mistura de calda.



EMBRAPA. Tecnologia de Produção de Soja – região central do Brasil – 2009. Londrina: Embrapa Soja: Embrapa Cerrados: Embrapa Agropecuária Oeste, 262p. 2008.
MaisSoja. Mosca branca: Soja e Algodão - 2019. Disponível em: https://www.youtube.com/watch?v=fSkkC3pFRlI
Pereira, M.F.A; Boiça JR, A.L.; Barbosa, J.C. Amostragem sequencial (Presença-Ausência) para Bemisia tabaci (Genn.) biótipo B (Hemiptera: Aleyrodidae) em feijoeiro (Phaseolus vulgaris L.). Neotropical entomology, v. 33, n. 4, 499-504, 2004.
Petroli, V. Infestação de mosca-branca causa perdas de até cinco sacas de soja por hectare em Mato Grosso na safra 16/17.


Marcos Roberto Conceschi, Pesquisador em Microbiologia Bionat
Álefe Vitorino Borges, Analista de Desenvolvimento de Mercado Bionat
Igor Henrique Sena da Silva, Analista de Desenvolvimento de Mercado Bionat

Receba por e-mail as últimas notícias sobre agricultura
Por Willian Damas, Especialista Agronômico Netafim
Para médias e grandes propriedades, colhedoras John Deere S 770, Case IH 7150, Valtra BC 7800, Massey Ferguson 9795 e New Holland CR Evo 7.80, comparadas pela Cultivar, possuem tecnologias e sistemas que satisfazem produtores exigentes